伦理审查线上申请流程
为提高临床研究伦理文件送审/备案递交效率,我院于2024年5月27日起,全面启用伦理审查信息系统,且配备有相应的CA电子签名功能,器械/药物注册类临床试验、临床科研项目、医疗新技术新项目、课题预审查等均可通过系统申请伦理审查,线上申请流程如下:
一、伦理审查信息系统登录网址
外网:https://erms.xmheart.com
内网:http://192.168.112.68:9988;或者内网登录OA--右侧“快捷功能”栏--伦理审查信息系统
二、账号、密码
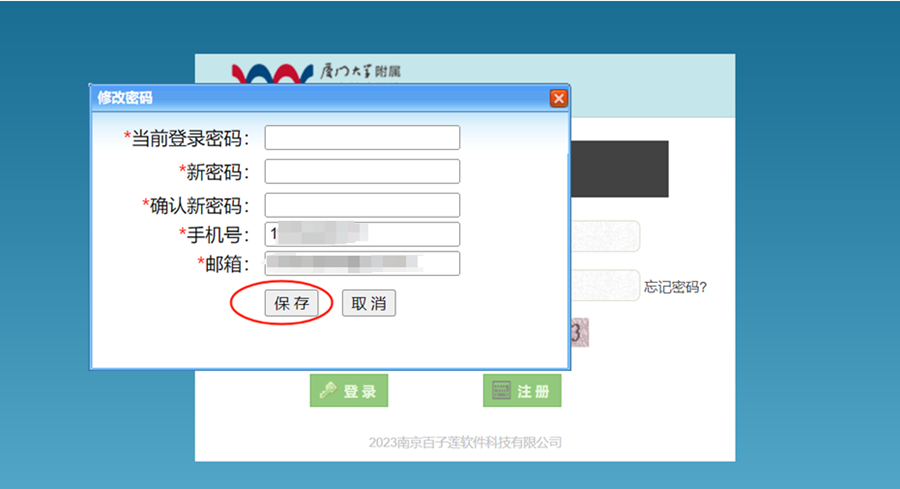
1、本院人员,可直接登录,首次登录需修改密码,并完善个人信息,其中,填写的手机号码需与注册CA电子签的手机号码一致;
用户名:工号(字母大写)
初始密码:XDxxg000
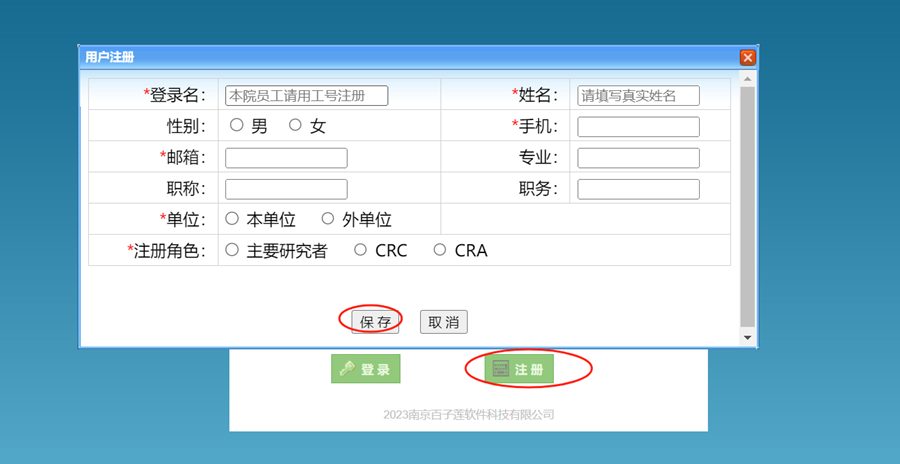
2、非本院人员,请先注册,同时将人员备案材料扫描件发送至伦理邮箱,然后联系伦理办公室审核授权后方可使用;
用户名:建议使用“CRA/CRC等角色名称+姓名”注册
初始密码:XDxxg000
三、申请流程(请注意查看每个界面顶部的红色提示说明)
(一)初始审查
1、主页面--新项目 或 主页面--项目管理--项目信息--新增 项目;
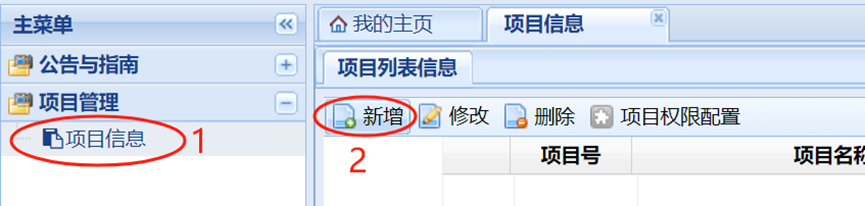
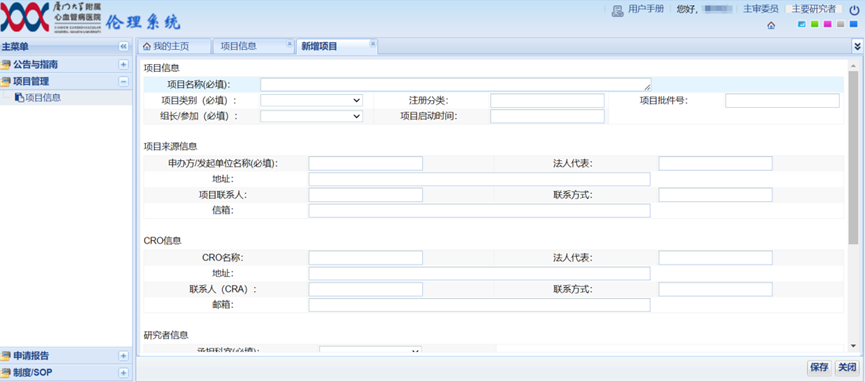
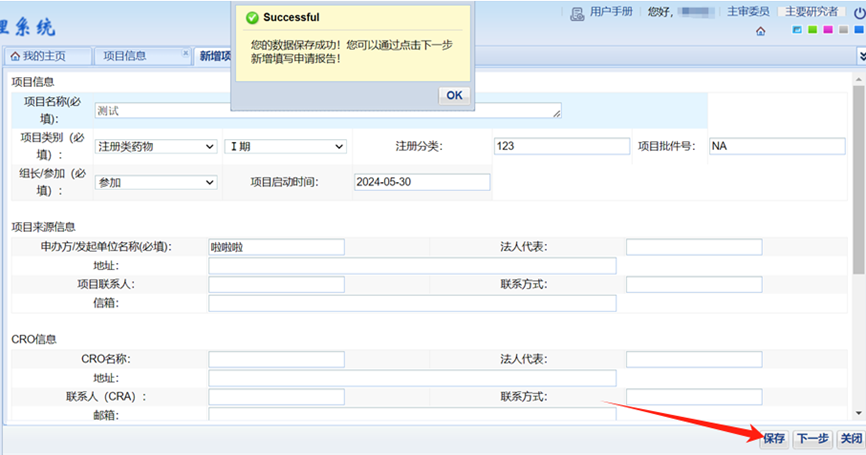
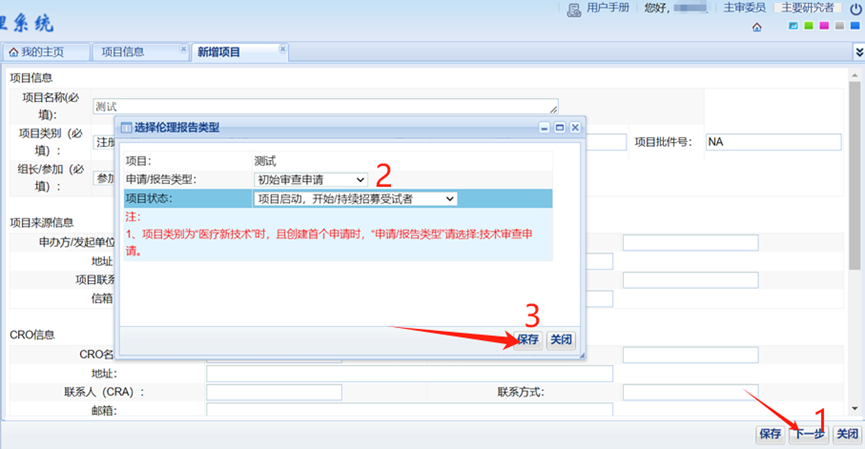
2、按照页面提示,完整填写项目相关信息,保存--下一步;
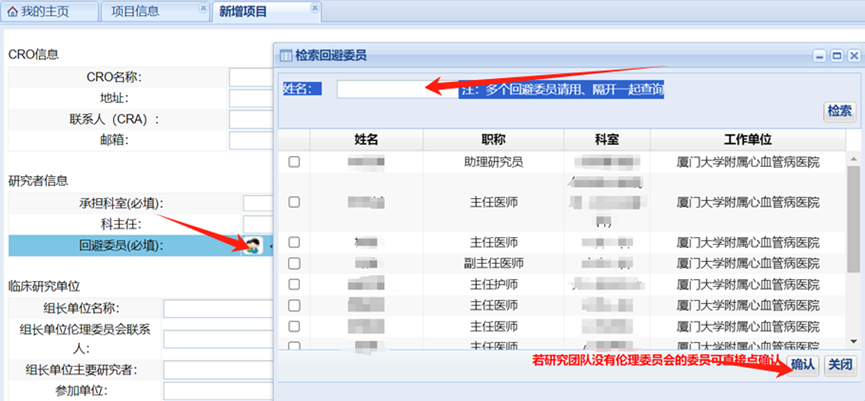
注意:若没有“回避委员”,请点击图标后,直接点“确认”即可;
3、申请/报告类型,选择“初始审查申请”;
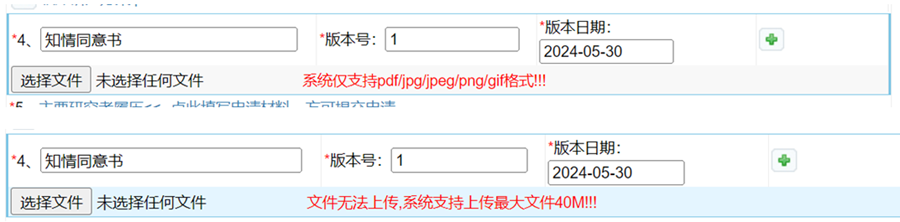
4、线上填写相应的申请表格等,并上传所需审查文件;
注意:请确保文件命名、版本号及日期的准确,此处填写的相关信息在系统内直接关联至最终的伦理审查意见/批件的目录,请勿必认真核对;系统仅支持pdf、图片格式,如果一种类型下的送审文件有多个文件则可以点击右边的“+”号进行添加,单个文件需要在40M之内;
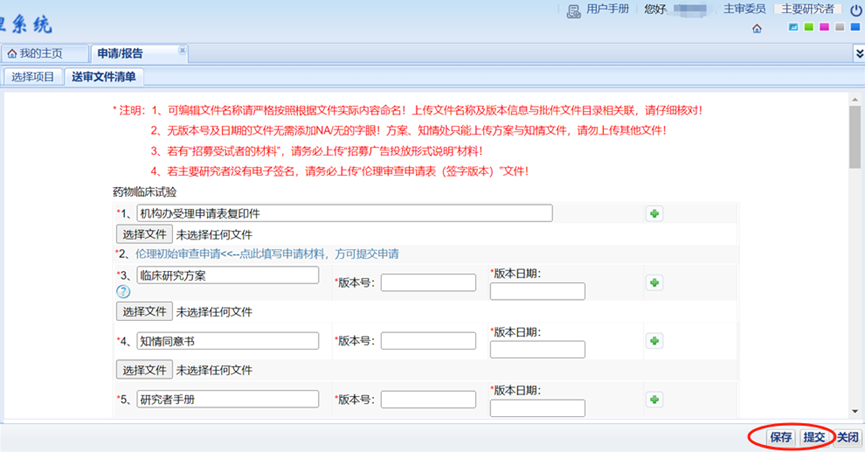
5、如您是主要研究者,可直接点击“提交”--医网信扫码签字--完成(图一);如您不是主要研究者,请点击“保存”,后联系主要研究者登录本系统审核提交(①主页面--待办事项--查看--提交--医网信扫码签字--完成;②主页面--申请报告--申请/报告--项目名称--提交--医网信扫码签字--完成)(图二);
注意:若研究者无CA电子签,请于系统中填写完整后,下载需签字文件,线下签署后上传扫描件;
图一:
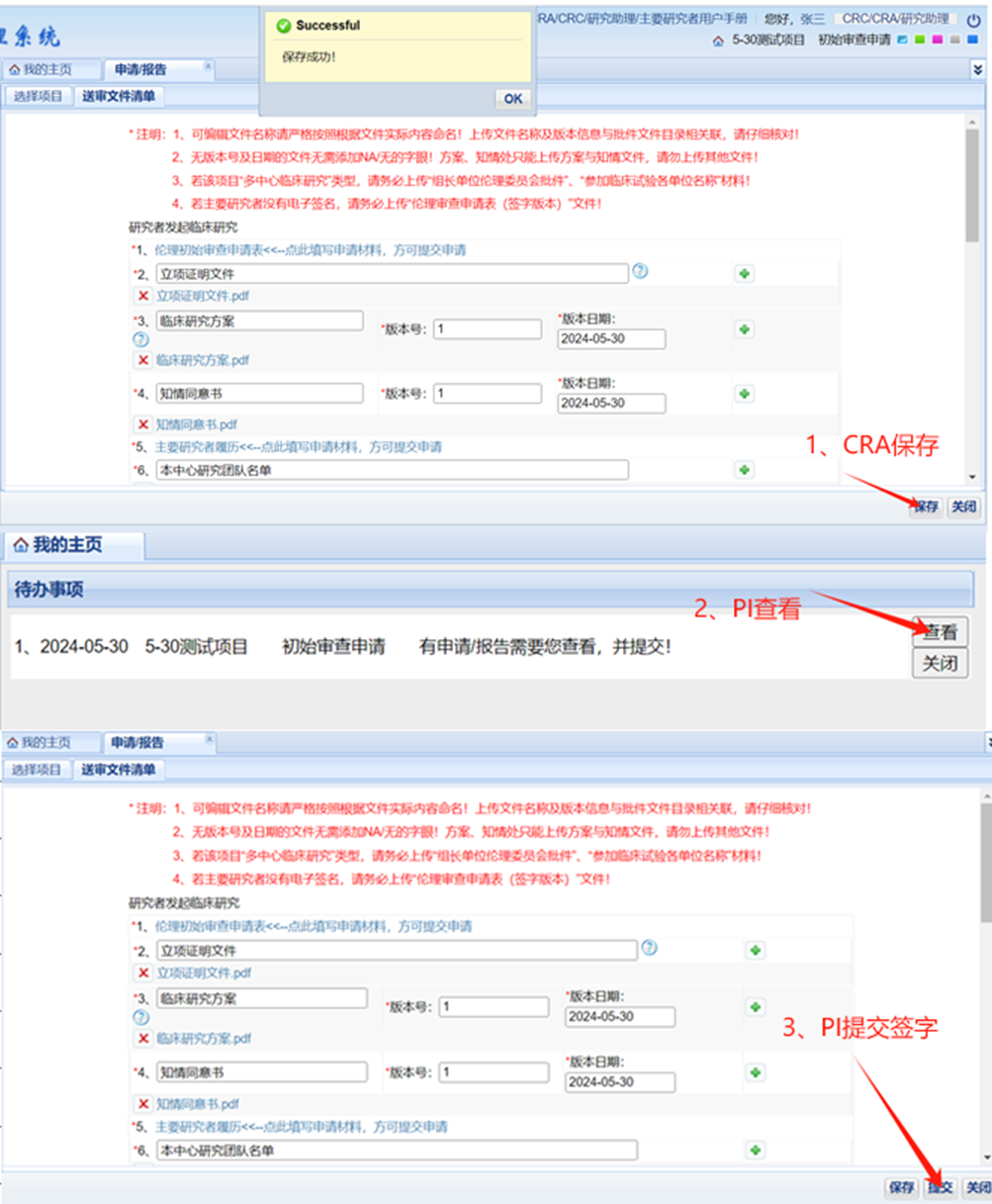
图二:
(二)其他审查类别
1、主页面--新伦理申请--选择项目--选择申请/报告类型--保存 或 主页面--申请报告--申请/报告--选择项目--选择申请/报告类型--保存
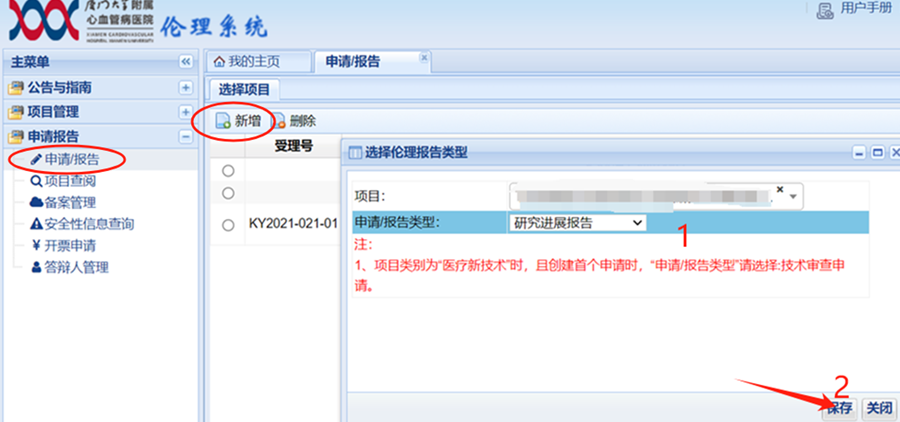
2、线上填写相应的申请表格等,并上传所需审查文件(同初始审查);
3、如您是主要研究者,可直接点击“提交”;如您不是主要研究者,请点击“保存”,后联系主要研究者登录本系统审核提交(同初始审查,本中心SAE可由授权的sub-I审核提交);
四、受理流程
1、办公室人员在1-3个工作日返回形式审查意见:补充/修改送审材料通知,或受理通知(带有正式受理号);
注意:对返回的形审意见,如有疑问,可线下与伦理办进一步咨询、沟通;
2、如有“补充/修改送审材料”意见,系统中将生成待办事项,申请创建人将同步接收到短信提醒,受理进度也可在伦理审查信息系统查询,请根据意见修改后再次提交;
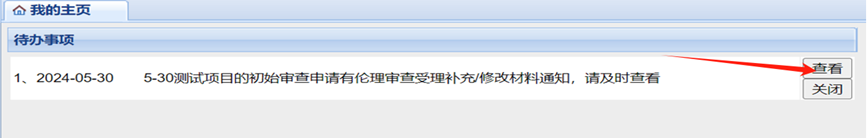
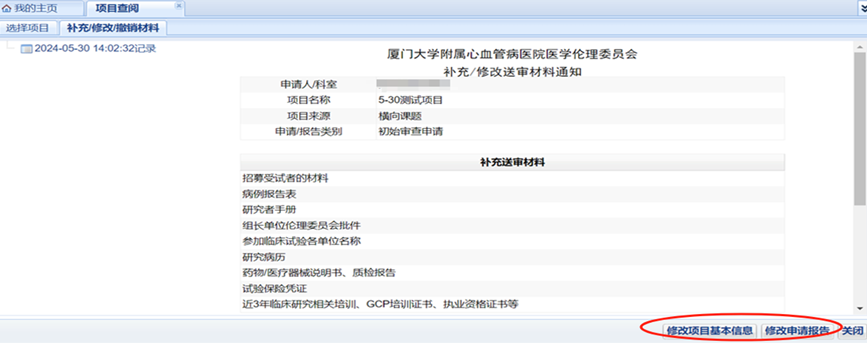
3、如收到“受理通知”,请根据通知要求下载打印完整材料一份,递交至伦理办公室,完成纸质受理;
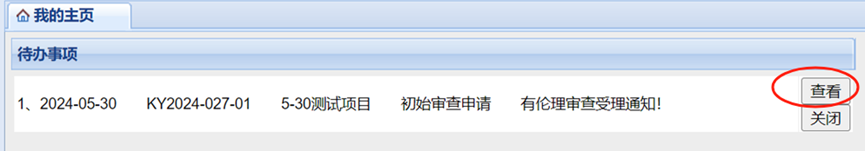
五、审查及结果反馈
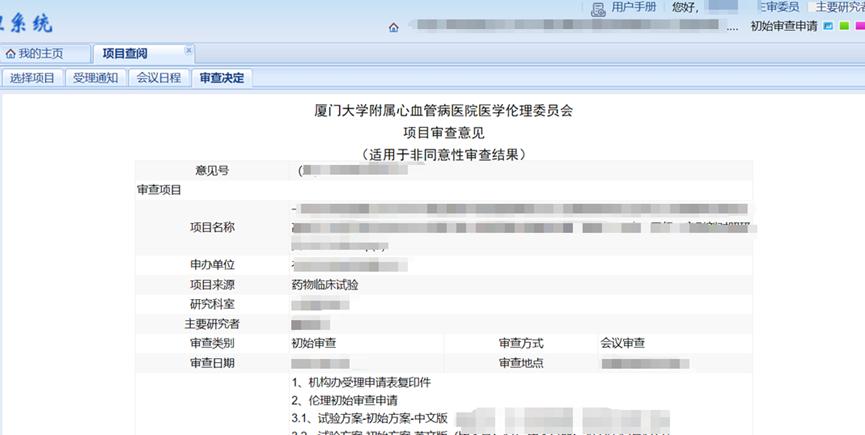
1、快速审查:受理后约5个工作日出具书面审查结果,可在“主页面--待办事项”中直接查看并下载,非同意性意见将同步发送短信提醒(请按意见修改后提交复审申请);
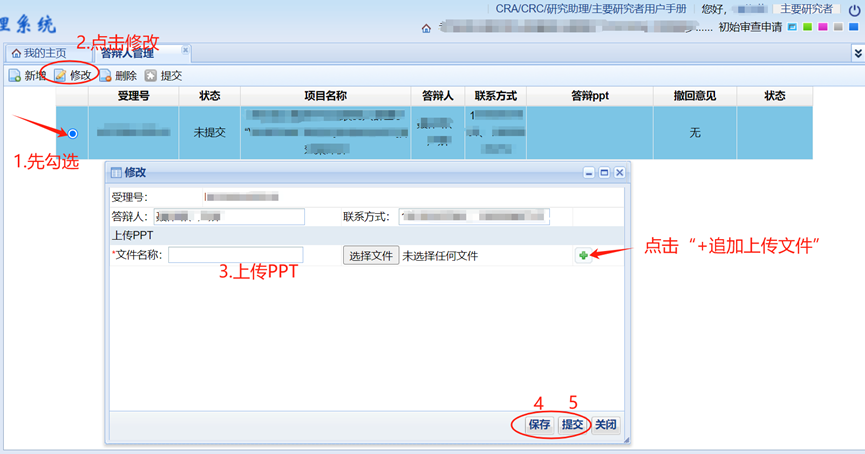
2、会议审查:受理后根据会议安排,请及时在系统中“申请报告--答辩人管理”填写答辩人信息并上传汇报PPT,会审后3-5个工作日出具书面审查结果,可在“主页面--待办事项”中直接查看并下载,非同意性意见将同步发送短信提醒(请按意见修改后提交复审申请)。